 Agentia americana pentru Controlul medicamentelor (FDA) a aprobat lansarea pe piata a medicamentului antiretroviral Truvada, primul tratament pentru prevenirea imbolnavirii cu SIDA destinat persoanelor cu risc si care ar trebui sa contribuie, potrivit autoritatilor, la reducerea de noi infectari. In urma unei recomandari a unui comitet de experti, aprobarea s-a dat ”cu scopul de a reduce riscul de transmitere a virusului SIDA (HIV) la subiecti sanatosi supusi unui risc ridicat de a fi contaminati”.
Agentia americana pentru Controlul medicamentelor (FDA) a aprobat lansarea pe piata a medicamentului antiretroviral Truvada, primul tratament pentru prevenirea imbolnavirii cu SIDA destinat persoanelor cu risc si care ar trebui sa contribuie, potrivit autoritatilor, la reducerea de noi infectari. In urma unei recomandari a unui comitet de experti, aprobarea s-a dat ”cu scopul de a reduce riscul de transmitere a virusului SIDA (HIV) la subiecti sanatosi supusi unui risc ridicat de a fi contaminati”.
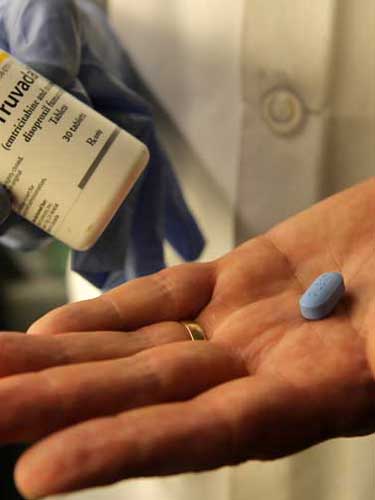
Truvada, luat zilnic, este destinat utilizarii in scop profilactic inainte de un contact sexual cu un partener avand virusul HIV (virusul imunodeficientei umane), in combinatie cu practici sexuale sigure, cum ar fi utilizarea prezervativului si de alte masuri de prevenire – screening periodic si tratarea altor boli venerice – pentru a preveni transmiterea HIV la adulti supusi unui risc ridicat de imbolnavire, dupa cum au precizat reprezentantii agentiei. Totusi, Truvada nu poate inlocui practicile sexuale sigure, a semnalat FDA.
Aprobarea FDA survine chiar inainte de Conferinta Internationala privind SIDA care va avea loc la Washington in perioada 22-27 iulie. ”In fiecare an, aproximativ 50.000 de adulti si adolescenti americani sunt diagnosticati cu HIV in pofida metodelor de prevenire, a strategiilor educationale, a testelor de depistare si a tratamentului pentru persoanele care au acest virus”, a declarat directoarea FDA, Margaret Hamburg.
Obiectivul in SUA este de a reduce numarul de noi infectii cu 25% pana in 2015, a afirmat dr. Debra Birnkrant, director al diviziei de produse antivirale din cadrul FDA.
Costul acestui tratament variaza intre 12.000 si 14.000 de dolari pe an.
Foto: Truvada (c) news.discovery.com
Sursa: Agerpres












 – Servicii de creare site web
– Servicii de creare site web
